有关实验室用的去污剂的全面综述,及其在生物医学实验中的应用。内容包括来邦网的文献调查结果。
A comprehensive review of laboratory detergents, and their applications in biomedical experiments, including Labome survey results.
在生物学或生物化学实验室使用的去污剂都是作用比较温和的表面活性剂(=表面活性成分),是用来破坏细胞膜(裂解细胞)以释放细胞内的可溶性物质。它们可以破坏蛋白质-蛋白质、蛋白质-脂质、脂质-脂质之间的连接,使蛋白质发生结构上的变性,防止蛋白质结晶,另外在免疫学实验中还可避免非特异性吸附。
实际应用中有众多不同的去污剂可以选择。为了某些特殊的应用,新的去污剂被不断开发出来 [1] 。在这篇综述中,对一些最常用的去污剂的特点和应用进行了论述。
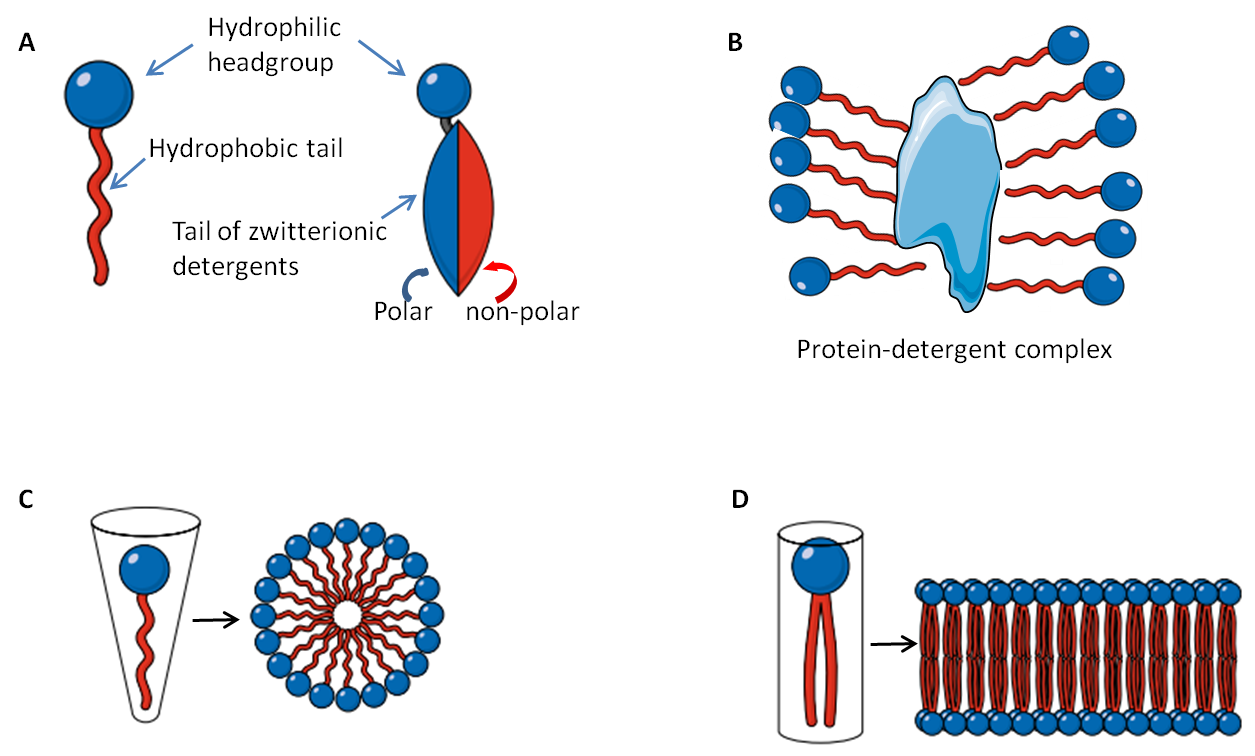
去污剂是由一个疏水尾端基团和一个极性亲水头端基团组成的有机化合物(图一A)。在一定的温度条件下,以特定浓度溶解于水时,去污剂分子会形成胶束,疏水基团部分位于胶束内部,而极性亲水基团则在其外部(图一B)。因此,胶束的疏水中心会结合到蛋白的疏水区域。一个胶束中,去污剂分子的聚集数目,是用来评价膜蛋白溶解度的一个重要参数 [2] 。去污剂分子疏水区域的长度和其疏水性成正比,且去污剂的疏水区域非常恒定,而极性头端亲水基团是可变的,可据其特点,把去污剂分为三类:离子型(阴离子或阳离子型),两性离子型和非离子型(见表一)。在特定的温度下,表面活性剂分子缔合形成胶束的最低浓度,称之为临界胶束浓度(CMC)。当去污剂低于临界胶束浓度时,只有单体存在;当高于临界胶束浓度时,胶束、单体以及其余不溶于水的非胶束相共存。同样,胶束形成的最低温度称为临界胶束温度(CMT)。因此,温度和浓度是去污剂两相分离和溶解性的重要参数。一般来说,低亲脂或憎油的去污剂的临界胶束浓度会较高。
| 种类 | 化合物 |
|---|---|
| 离子去污剂 | 十二烷基硫酸钠(SDS),脱氧胆酸钠, 胆酸钠, 肌氨酸 |
| 非离子去污剂 | triton X-100, 十二烷基麦芽糖苷,洋地黄皂苷, tween 20, tween 80 |
| 两性离子去污剂 | CHAPS |
| 离液剂 | 尿素 |
离子去污剂是由一个疏水链和一个阳离子或阴离子的极性头端基团组成。此类去污剂的临界胶束浓度一般高于非离子去污剂。此类去污剂活性较强。由于离子去污剂存在极性头部基团,因此不能通过离子交换色谱法去除。
SDS是一种非常高效的表面活性剂,几乎可以使所有的蛋白质溶解。它可以破坏蛋白质的非共价键,从而使蛋白质变性,并丧失天然构象和功能。SDS以质量比1.4:1与蛋白质结合(或一个SDS阴离子结合二个氨基酸分子),因此即使蛋白质样品处于等电点,SDS也能掩饰蛋白质的带电情况,使其带负电。这是被广泛使用的变性聚丙烯酰胺凝胶电泳的原理所在。通常,为了在SDS存在时完全裂解细胞,样品必须经过超声处理或若干次通过19G的针头,从而确保DNA的完全降解。SDS会使蛋白质变性并破坏其三维结构,因此当研究中需要蛋白质的活性或蛋白质的相互作用存在时,不能使用SDS。当使用离子去污剂时,此外还要注意一些事项,因为在不同离子强度的缓冲液中,它们的特性会随之改变(比如说,当氯化钠浓度从0增加到500mM时,去污剂的临界胶束浓度会从8mM降至0.5mM)。另外,SDS在温度较低时会发生沉淀,这是因为它属于去污剂中临界胶束温度最高的一种,而且这种沉淀现象在钾盐存在的情况下会更加明显。SDS的这种特性可以用来去除蛋白质样品中的SDS [3] 。
脱氧胆酸钠和胆酸钠即使没有一个极性头端基团,但是也归入离子去污剂的类别,是因为它们的极性基团分布在分子链的各个部分。它们可以用来溶解细胞膜。
十二烷基肌氨酸钠(Sarkosyl 或Sarcosyl)也叫月桂酰肌氨酸钠,是一种阴离子表面活性剂。它具有两亲性,既有疏水的14碳链(月桂酰)也有亲水的羧基。酰胺键的氮原子没有pH活性且不受pH变化影响而保持中性。羧基的pKa值为3.6,在生理条件下带负电。此外,在宽范围的pH下肌氨酸的表面活性都非常高,表面张力约为3.4 × 10–2 到2.9 × 10–2N/m。
Sarkosyl是在氢氧化钠存在下由月桂酰氯和肌氨酸反应,通过乙醇重结晶或矿物酸酸化、游离酸分离和中和纯化而得。文献中使用的Sarkosyl通常来自Sigma。最常用的商品形式是30%的水溶液。
Sarkosyl经常用于洗发水、沐浴露、洗面奶和表面活性剂清洁剂等化妆品配方中。气相色谱分析标明Sarkosyl在肥皂中用量在2.78-12.9% [4] 。Sarkosyl在金属表面处理工业中用于晶体改性、防锈和抗腐蚀。Sarkosyl还被用于改善局部药物的浸润和渗透。在食品工业,Sarkosyl被批准用于人用食品的处理、包装和运输,还可作为交联剂用于食品的储存和运输。
Sarkosyl因良好的水溶性、高泡沫稳定性和对蛋白强吸附能力等优点被广泛应用于实验研究。它可以抑制DNA转录的启动。作为去污剂,Sarkosyl可以渗透细胞,在蛋白的分离纯化技术中用于蛋白提取,比如免疫印记和间接ELISA。
Sarkosyl的一个主要应用是从包涵体中溶解和重折叠蛋白。在大肠杆菌(Escherichia coli)中过表达的真核重组蛋白倾向于形成包涵体。Sarkosyl可以从包涵体中提取自然折叠的蛋白。通常一个包涵体颗粒溶于0.3%的Sarkosyl。10%Sarkosyl与包涵体孵育可以有效溶解超过95%的蛋白,通过特定比例的Triton X-100和CHAPS可以高产率地回收Sarkosyl溶解的融合蛋白 [5] 。早期工作包括使用尿素和盐酸胍等变性剂溶解包涵体,再通过缓慢稀释重折叠。然而,一旦去除强去污剂,绝大部分溶解的蛋白会立即聚集并沉淀。现已发现Sarkosyl是一种有效的增溶剂,可以在更高的蛋白浓度下重折叠(与盐酸胍相比高10倍 [6] )。此外,Sarkosyl在进行溶解蛋白重折叠时,蛋白聚集比尿素和盐酸胍更少。在亲和纯化前,在4°C下蛋白在含Sarkosyl的可溶性提取剂中可以储存一周。但是Sarkosyl会干扰随后的色谱过程,因此必须通过稀释或者透析去除。
非离子型去污剂和离子型不同,它们的头端基团是没有极性的亲水基团。它们被认为是比较温和的表面活性剂,它们可以破坏蛋白质-脂质以及脂质-脂质之间的连接,但是不能破坏蛋白质-蛋白质的连接,而且大多非离子去污剂不能使蛋白质变性。因此,这种去污剂可以使蛋白质溶解和分离,但却保留了蛋白质的天然构象、功能以及它们的相互作用。在分离膜蛋白的应用中,这是此类去污剂的优势所在。新型非离子型去污剂如糖基石胆酸酯两亲分子(GLC-1,GLC-2和GLC-3)和糖酵素(GDN)也有报道 [7] 。GDN用于从酵母线粒体膜提取ATP合成酶二聚体 [8] 。
Triton X-100是一个非离子表面活性剂的重要代表,并应用于大多免疫沉淀实验中。这个家族的所有成员(Triton X100, Triton X114, Nonidet P40, Igepal CA-630) 非常相似,仅仅在每个胶束(分别为9.6, 8.0, 9.0 and 9.5)的平均单体数量和基于PEG的头端基团的大小分布上有区别 [9] 。Triton X100来源于聚氧乙烯,并含有一个烷苯基疏水基团。Triton X100临界胶束浓度较低,因此不易通过透析法去除。其浊点是64摄氏度,在此温度下,可以观察到两相分离。
十二烷基麦芽糖苷(DDM)是一种糖苷表面活性剂,越来越多地被用来分离需要保留活性的疏水性膜蛋白。已证明在此应用中,DDM比CHAPS或NP-40要高效地多 [10] 。DDM糖链的亲脂位点、0.17mM的高临界胶束浓度以及在胶束界面形成的水样的微环境,这对于溶解和保持细胞膜疏水蛋白的稳定性非常关键。
其它麦芽糖苷有不同长度的疏水烷基链,比如β-癸基麦芽糖苷。葡萄糖苷(比如辛基葡萄糖苷)也可以用于蛋白实验 [11-13] 。
从紫色毛地黄(洋地黄紫癜)中提取,可以用于分离真核细胞膜疏水蛋白。肌氨酸和Triton X-100可以溶解细菌内部蛋白,但不是外部的细菌胞膜。
Tween-20和Tween-80是具有脂肪酸的酯基团和长聚氧乙烯链的聚山梨酯表面活性剂。它们临界胶束浓度很低,一般都是温和的表面活性剂,不仅不影响蛋白质活性,而且溶解蛋白的能力也高。它们不是细胞裂解液的常见组分,但是通常见于免疫印迹和酶联免疫吸附实验中的洗涤缓冲液,因为它们可以最大程度地减少非特异性结合的抗体以及去除不结合的部分。
关于Tween家族去污剂的一个常见问题是两种最常见成员Tween-20和Tween-80的差别。Tween-20有月桂酸基团,Tween-80有油酸基团(图3)。表二总结了它们不同的特点。这些差别有时非常重要,尤其是在活体研究中,因为Tween-20和Tween-80溶血作用不同 [14] 。
| 别名 | 化学式 | 分子量 | 密度(g/mL) | 外观 | 应用 | |
|---|---|---|---|---|---|---|
| Tween 20 | 聚山梨醇酯20,聚氧乙烯脱水山梨糖醇单月桂酸酯,PEG(20)脱水山梨糖醇单月桂酸酯 | C58H114O26 | 1228 | 1.1 | 透明,黄色至黄绿色粘稠液体 | 应用广泛: 作为PBS或TBS洗涤缓冲液的封闭剂用于ELISA、免疫印记和其它免疫方法, 哺乳动物细胞裂解,膜蛋白的助溶剂。 |
| Tween 80 | 聚山梨醇酯80,聚氧乙烯脱水山梨糖醇单月桂酸酯,PEG(80)脱水山梨糖醇单月桂酸酯 | C64H124O26 | 1310 | 1.06-1.09 | 琥珀色粘稠液体 | 蛋白稳定剂,鉴定某些分枝杆菌表型的试验。 |
大多数离子去污剂会干扰紫外线(UV)分光光度法,特别是Triton X100,因为此类去污剂都含有一个可以吸收紫外线的苯环。因此,280nm紫外线波长下检测蛋白质吸光度会变的不准确。
两性离子去污剂 头端基团是亲水性,含有正负电荷各一个,因此呈现电中性。它们一般是比非离子型更强烈的表面活性剂。最典型的例子是3-(3-(胆酰胺丙基)二甲氨基)丙磺酸内盐,更常称为CHAPS。它的临界胶束浓度(室温下6mM)高,可以通过透析的方法高效去除。在2-4%浓度的等电聚焦和二维电泳的样品制备中,经常使用。CHAPSO和CHAPS不同,CHAPSO含有一个极性更强的头端基团,可以使它的可溶性更高。因此,CHAPSO可以用于完整细胞膜蛋白的溶解。
各类离液剂是同类物质的表面活性剂,它们可以打破非共价的相互作用(氢键,偶极-偶极相互作用,疏水相互作用),使蛋白质发生可逆性变性。单独使用尿素,或与硫脲或其它去污剂联合使用,在二维电泳或在蛋白组学研究中配制蛋白质的酶消化液中广泛使用。此外,在使用尿素的时候需注意不能加热样品至37摄氏度以上,这会导致蛋白质的氨甲酰化 [15] 。
很多人对膜蛋白的分离比较感兴趣,但是分离膜蛋白和分离胞质蛋白、胞核蛋白不同,会出现一些特殊的问题。主要原因有膜蛋白表达水平低且很难溶于水溶液,细胞膜具有比较复杂的脂质层及亲水、疏水区域。为了提高膜蛋白的溶解性,首先应该选择临界胶束浓度较高的去污剂,另外缓冲液的体积也要足够大,这样才可以加足够多的去污剂去溶解样品中所有的膜蛋白。根据此链接 [2] ,每一个膜蛋白分子至少需要一个胶束,这样才足以模拟细胞膜的脂质环境(图1C-1D)。原则上,通过调整温度和缓冲液中的盐浓度,以及利用去污剂的两相分离的特性,可以使膜蛋白有效地溶解。此时,被胶束包绕的膜蛋白和去污剂一起发生沉淀,可溶性蛋白保留在上清中。去污剂缓冲液出现两相分离的温度,称之为浊点。除了温度的影响,浊点还受缓冲液中其它一些因素的影响,比如甘油和盐类(例如,Triton X114的浊点是23摄氏度,但是如果在去污剂缓冲液中添加了20%的甘油,浊点会降到4摄氏度)。当某个蛋白质的稳定性受高温影响时,这就显得非常重要。
良好的去污剂首先应该能够充分裂解细胞,溶解其中的蛋白,并对后续的实验研究没有影响。对于想要得到保留天然构想的还是变性的蛋白质,这才是第二考虑的问题。没有一种去污剂可以适用于所有的实验研究,即使应用于同一种实验技术,去污剂效果的好坏还取决于实验所分离的蛋白质(表格三)。因此,通过尝试和失败经验,可以帮助我们找到最合适的去污剂,此外,还可以尝试使用去污剂的混合物。需要再强调的是,配置新鲜的去污剂缓冲液也很重要,可以防止久置的去污剂缓冲液发生水解和氧化。
| 去污剂 | 单体分子量 Da | 胶束分子量 Da | 临界胶束浓度 (mM) 25℃ | 聚集数 | 浊点 (℃) | 平均胶束质量 | 强度 | 透析(去除) | 应用 |
|---|---|---|---|---|---|---|---|---|---|
| 十二烷基硫酸钠(SDS) | 289 | 18,000 | 7-10 | 62 | >100 | 18,000 | 强烈 | 是 | 细胞裂解, 电泳, WB, 杂交 |
| Triton X-100 | 625 | 90,000 | 0.2-0.9 | 100-155 | 65 | 80,000 | 温和 | 否 | 酶联免疫测定, IP, 溶解膜蛋白 |
| 3-((3-胆固醇氨丙基)二甲基氨基)-1-丙磺酸(CHAPS) | 615 | 6,150 | 6 | 10 | >100 | 6,150 | 温和 | 是 | IEP, IP |
| 乙基苯基聚乙二醇(NP-40) | 680 | 90,000 | 0.059 | 45-50 | 温和 | 否 | IEP | ||
| 十二烷基麦芽糖苷(DDM) | 511 | 0.15 | 98 | 50,000 | 蛋白结晶 | ||||
| Tween-20 | 1228 | 0.06 | 76 | 温和 | 否 | WB, 酶联免疫吸附法, 酶联免疫测定 | |||
| 洋地黄皂苷 | 1229 | 70,000 | <0.5 | 60 | 70,000 | 温和 | 否 | 溶解细胞膜 |
残留去污剂的类型及浓度多少会对实验有一定影响,因此通常需要降低或者清除残留的去污剂。为了实现此目标,可以使用尺寸排阻层析法或者透析法,但这基于胶束大小要不同于所分离的蛋白质分子大小,或者胶束要小(例如比较高的临界胶束浓度)到可以通过透析管 [2] 。此外,还可使用非极性微球或树脂结合去污剂、环糊精包合物 [16] ,使用离子交换色谱法或蛋白质沉淀法。但是,在去除去污剂后,要格外注意防止蛋白质的沉淀和聚集。
来邦调查了关于去污剂应用的相关文献。下列表格列出了去污剂的主要供应商及被应用的论文数目,可以发现大多去污剂都是来源于Sigma Aldrich公司。
| 去污剂 | 数目 | 供应商 |
|---|---|---|
| Triton X-100 | 34 | Thermo Fisher, Amresco, JT Baker, Packard, Sigma |
| Tween-20 | 19 | Thermo Fisher, Amersham Pharmacia, Bio-Rad |
| 十二烷基硫酸钠(SDS) | 13 | Amresco, Bio-Rad, Q.BIOgene, Sigma |
| 乙基苯基聚乙二醇(NP-40) | 6 | Roche, Sigma |
| 3-[(3-胆固醇氨丙基)二甲基氨基]-1-丙磺酸(CHAPS) | 6 | EMD Millipore/Merck/Calbiochem, Sigma, JT Baker |
| 洋地黄皂苷 | 8 | EMD Millipore/Merck, Sigma |
Thermo Fisher Pierce公司的Triton X-100常用来裂解细胞或组织样品以用于免疫印迹实验 [17, 18] 和免疫细胞化学 [19] 。来自Amresco公司的30%TritonX-100可以用于大鼠脊髓组织的匀浆 [20] 。JT Baker公司的Triton X-100可用于细胞的固定和破膜,从而使肌动蛋白骨架可见 [21] 。Packard的Triton-X用来溶解免疫组织化学技术中的一抗 [22] 。Sigma的Triton X-100,用于免疫组织化学技术中细胞的破膜 [23-31] 、封闭液的配制 [32-35] ,用于免疫印迹实验中细胞或组织样品的裂解和蛋白质的溶解 [36, 37] ,还可应用于PCR实验 [38] 、脂质体融合实验 [39] 、染色实验 [12] 。
在各种免疫学实验中,Tween-20经常用于洗涤缓冲液中,例如TBS-T,PBS-T。Fisher公司的0.05% Tween可用于酶联免疫吸附实验 [40] 。Amersham Pharmacia的Tween 20可用于免疫印迹实验 [41] 。来源于Bio-Rad的Tween 20可用来配制PBS-T缓冲液,用于免疫印迹实验 [37] 或用于免疫组织化学实验中洗涤组织切片 [42] 。Sigma公司的Tween-20可以用于免疫印迹 [25, 37], [43], [44], [45-48] 、酶联免疫吸附 [49, 50] 、免疫共沉淀 [48] 、原位杂交 [49] 、多重PCR [50] 或其它实验技术 [51, 52] 。
Amresco公司的SDS可用于SDS-聚丙烯酰胺凝胶电泳 [53] 。Bio-Rad的十二烷基硫酸钠的可用来制备放射免疫沉淀实验中的分析缓冲液 [51] 。Q.BIOgene的SDS可用于免疫印迹实验中的缓冲液配制 [52] 。SIGMA的SDS可用于制备体外辛酰化、Laemmli样品及2D-DIGE实验的缓冲液 [37, 51, 54-61] 。
Roche公司的NP-40可用于裂解细胞 [62, 63] 。Sigma的NP-40可用于制备放射免疫沉淀实验中的缓冲液 [51] 、细胞裂解液 [60] 、以及免疫共沉淀实验中的RIPA缓冲液 [31] 。
来自Calbiochem的CHAPS(2%,质量体积比)可以用于鉴定卵巢癌的循环蛋白标记物的实验中 [40] 。Sigma公司的CHAPS可用于制备纯化小鼠重组蛋白proghrelin的缓冲液 [64] 、免疫共沉淀的缓冲液 [31] 、裂解组织的缓冲液 [62] 。JT Baker的CHAPS可用余裂解细胞以研究人ASF1蛋白分子与病毒的相互作用 [65] 。
MERCK公司的洋地黄皂苷可以用于免疫细胞化学实验中,以研究质膜中PI4P的作用 [66] 。Sigma的洋地黄皂苷可用于细胞破膜,以研究上皮细胞和间充质细胞对大肠杆菌Shiga毒素1的反应 [67] ,研究自噬 [68] ,还可用于制备提取液,以研究TNF-alpha对巨噬细胞的作用 [69] ,进行蛋白酶K保护实验 [70] 以及RNA提取 [71] 。Wako的洋地黄皂苷被用于细胞裂解 [72] 以及免疫沉淀实验 [73] 。
Anatrace的正癸基-β-D-吡喃麦芽糖苷(5mM)被用于蛋白纯化 [74, 75] ,该公司的正十二烷基-β-D-麦芽糖苷 [76-80] 和正十一烷基-β-D-麦芽糖苷 [79, 81] 也可以用于蛋白纯化。Glycon的β-十二烷基麦芽糖苷和β-癸基麦芽糖苷也可用于蛋白纯化 [13] 。Sigma的正十二烷基-β-麦芽糖苷(1%浓度)用于胰蛋白酶裂解抑制实验 [82] ,癸基麦芽糖苷被用来进行蛋白分离 [83] 。
Glyconde的辛基葡萄糖苷被用于蛋白纯化 [12] 和标记 [13] 。Anatrace的正辛基-β-葡萄糖苷被用于脉冲追踪分析 [11] 。
纯化蛋白时,Affymetrix辛基糖新戊二醇(OGNPG) [84] 可以用1%的浓度;Sigma的胆甾醇半琥珀酸酯可用0.1%(质量体积比)的浓度 [85] 。
- Suzuki H, Terada T. Removal of dodecyl sulfate from protein solution. Anal Biochem. 1988;172:259-63 pubmed
- Lanigan R. Final report on the safety assessment of Cocoyl Sarcosine, Lauroyl Sarcosine, Myristoyl Sarcosine, Oleoyl Sarcosine, Stearoyl Sarcosine, Sodium Cocoyl Sarcosinate, Sodium Lauroyl Sarcosinate, Sodium Myristoyl Sarcosinate, Ammonium Cocoyl Sarcosinate,. Int J Toxicol. 2001;20 Suppl 1:1-14 pubmed
- Burgess R. Purification of overproduced Escherichia coli RNA polymerase sigma factors by solubilizing inclusion bodies and refolding from Sarkosyl. Methods Enzymol. 1996;273:145-9 pubmed
- Arnold T, Linke D. Phase separation in the isolation and purification of membrane proteins. Biotechniques. 2007;43:427-30, 432, 434 passim pubmed
- Luche S, Santoni V, Rabilloud T. Evaluation of nonionic and zwitterionic detergents as membrane protein solubilizers in two-dimensional electrophoresis. Proteomics. 2003;3:249-53 pubmed
- Vinardell M, Infante M. The relationship between the chain length of non-ionic surfactants and their hemolytic action on human erythrocytes. Comp Biochem Physiol C Pharmacol Toxicol Endocrinol. 1999;124:117-20 pubmed
- Degrip W, VanOostrum J, Bovee Geurts P. Selective detergent-extraction from mixed detergent/lipid/protein micelles, using cyclodextrin inclusion compounds: a novel generic approach for the preparation of proteoliposomes. Biochem J. 1998;330 ( Pt 2):667-74 pubmed
- Zhou H, Yang H, Li Y, Wang Y, Yan L, Guo X, et al. Changes in Glial cell line-derived neurotrophic factor expression in the rostral and caudal stumps of the transected adult rat spinal cord. Neurochem Res. 2008;33:927-37 pubmed
- Peralta Ramirez J, Hernandez J, Manning Cela R, Luna Munoz J, Garcia Tovar C, Nougayrede J, et al. EspF Interacts with nucleation-promoting factors to recruit junctional proteins into pedestals for pedestal maturation and disruption of paracellular permeability. Infect Immun. 2008;76:3854-68 pubmed 出版商
- Castilow E, Olson M, Meyerholz D, Varga S. Differential role of gamma interferon in inhibiting pulmonary eosinophilia and exacerbating systemic disease in fusion protein-immunized mice undergoing challenge infection with respiratory syncytial virus. J Virol. 2008;82:2196-207 pubmed
- Chung Y, Troy H, Kristeleit R, Aherne W, Jackson L, Atadja P, et al. Noninvasive magnetic resonance spectroscopic pharmacodynamic markers of a novel histone deacetylase inhibitor, LAQ824, in human colon carcinoma cells and xenografts. Neoplasia. 2008;10:303-13 pubmed
- Salvi A, Bongarzone I, Miccichè F, Arici B, Barlati S, De Petro G. Proteomic identification of LASP-1 down-regulation after RNAi urokinase silencing in human hepatocellular carcinoma cells. Neoplasia. 2009;11:207-19 pubmed
- Dianzani C, Brucato L, Gallicchio M, Rosa A, Collino M, Fantozzi R. Celecoxib modulates adhesion of HT29 colon cancer cells to vascular endothelial cells by inhibiting ICAM-1 and VCAM-1 expression. Br J Pharmacol. 2008;153:1153-61 pubmed
- 来邦网
- 英文来邦